Swissmedic Publishes Updated Information Sheet on Medical Device Software (Version 3.0)
Swissmedic releases updated guidance on medical device software (MDSW), covering qualification, classification, and regulatory requirements under MDR/IVDR.
Swissmedic Updates CAPA Plan Content Requirements for Medical Devices
Swissmedic publishes updated CAPA plan requirements for medical devices, effective April 2026. Key impacts for manufacturers and compliance strategies explained.
Swissmedic updates guidance on clinical investigations of medical devices
Swissmedic releases updated guidance on clinical investigations of medical devices, clarifying Category A vs C studies, ISO 14155 compliance, and safety reporting requirements for manufacturers.
Swissmedic Issues Minor Update to Guidance on User Incident Reporting
Swissmedic updates guidance on medical device incident reporting. Key timelines, obligations, and implications for manufacturers explained.
Swissmedic Publishes “Good Practice for Materiovigilance in Hospitals” (GPMV-Spital)
Swissmedic releases GPMV-Spital, a new framework for materiovigilance in hospitals. Understand the impact on medical device manufacturers and post-market surveillance.
Swissmedic publishes updated guidance on Systems and Procedure Packs (SPP)
Swissmedic updates guidance on systems and procedure packs. Key obligations, CH-REP requirements, and impact for medical device manufacturers.
Swissmedic Updates “Formal Requirements” Guidance – Version 20.0 Now in Force
Swissmedic has released Version 20.0 of its “Formal Requirements” guidance, effective 1 March 2026. Learn what pharmaceutical manufacturers need to know about submission formats, documentation requirements and parallel import updates.
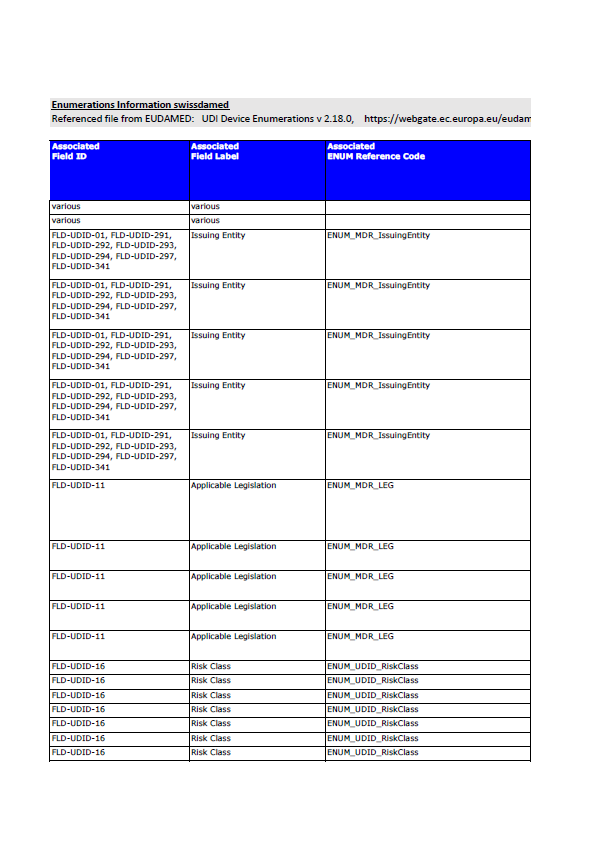
Swissmedic Updates swissdamed UDI Data Dictionary
Swissmedic has published version 3.0 of the swissdamed UDI Data Dictionary, introducing clarifications to SRN fields and new machine-to-machine attributes for improved data mapping.
Swissmedic Publishes swissdamed Machine-to-Machine REST API Documentation (Version 1.0)
Swissmedic publishes Version 1.0 of the swissdamed Machine-to-Machine REST API documentation for UDI registration and market status management.
Swissmedic Publishes Updated Online Help for the Medical Device Publication Service
Swissmedic has published version 1.2 of its guidance on the Medical Device Publication Service, clarifying how Field Safety Corrective Actions and Field Safety Notices are published and accessed.
Swissmedic Updates Formal Requirements Guidance – Version 19.0 Applicable from February 2026
Swissmedic has published version 19.0 of its Formal Requirements Guidance, applicable from February 2026. Learn what manufacturers and combination product developers need to prepare for.
Swissmedic Publishes Updated EUDAMED UDI Enumerations: What Manufacturers Should Know
Swissmedic publishes updated EUDAMED UDI enumerations (v2.18.0). What this means for manufacturers preparing UDI, device and certificate data submissions.
Swissmedic Updates eIAM Portal Administrator Guidance – Version 3.4 Effective February 2026
Swissmedic publishes eIAM Portal Administrator guidance version 3.4, effective February 2026. Learn what this means for manufacturers using Swiss eGov services.
Swissmedic Highlights Critical Deficiencies in Notified Body Opinions for Integral Combination Products
Swissmedic’s review of Notified Body Opinions under MDR Article 117 reveals major gaps in documentation quality for drug–device combination products. Updated expectations now apply to ensure compliance with GSPRs.
Swissmedic Updates swissdamed Business Rules – Key Changes for Device Manufacturers in 2026
Swissmedic has released version 3.0 of its swissdamed Business Rules, effective January 2026. The update includes stricter UDI-DI requirements, limits on legacy device data, and mandatory fields for MDR/IVDR submissions. Manufacturers must now align with Swiss-specific data rules diverging from EUDAMED.
Swissmedic Publishes New Guidance on Scientific GMDP Meetings for Establishment Licence Holders
New Swissmedic guidance formalises the process for Scientific GMDP Meetings with Swiss establishment licence holders. Effective January 2026. Download the official document here.
Swissmedic Updates Guidance on Export Certificates: Key Implications for Medical Device Manufacturers
Swissmedic has released updated guidance on the requirements for obtaining export certificates (Free Sales Certificates) for medical devices, introducing clearer rules for manufacturers on documentation, conformity evidence, product grouping, and submission procedures. The revised framework is essential for manufacturers exporting devices to global markets that require FSCs as part of their regulatory registration.
Swissmedic Reinforces Signal Management and PSUR Requirements for Veterinary Medicinal Products
Swissmedic’s updated guidance on PSUR Signal Management sets a higher standard for pharmacovigilance in Switzerland. By aligning with EU Regulation 2019/6 and VICH GL 29, it requires manufacturers to strengthen PSUR reporting, signal evaluation, and safety data traceability. For medical device and IVD producers, this shift underscores the importance of robust post-market surveillance and regulatory readiness. Smart MDR supports companies in navigating these evolving frameworks efficiently and confidently.
Swissmedic lança novo portal eletrónico para comunicações de segurança
A Swissmedic lançou o novo portal eletrónico de comunicações de segurança (eGov Safety Communication Service), uma ferramenta digital que permite a transmissão segura e encriptada de informações entre as empresas e a autoridade suíça de medicamentos e dispositivos médicos. Esta iniciativa visa simplificar os processos de conformidade, reduzir a carga administrativa e reforçar a vigilância pós-comercialização de dispositivos médicos e IVD. A Smart MDR destaca esta inovação como um exemplo de digitalização inteligente no setor da saúde, alinhada com as tendências europeias de modernização e eficiência na comunicação entre fabricantes e autoridades competentes.
Swissmedic publica orientações sobre o uso de tecnologias móveis em medicamentos
A Swissmedic publicou novas orientações sobre a utilização de tecnologias móveis em medicamentos, com especial foco nos códigos QR. O guia, em vigor a partir de agosto de 2025, define regras para garantir que a informação digital seja clara, acessível, segura e em conformidade legal, reforçando a segurança dos pacientes e o alinhamento com as práticas da EMA.